
前哨淋巴结活检(SLNB)与腋窝淋巴结清扫(ALND)相比具有并发症少和创伤小的优势[1],已经成为乳腺癌腋淋巴结外科重要的手术方式。然而在我国的临床实践中,依然有很多实际问题等待我们去解决。首先得到广泛认可的核素联合染料双示踪法[2],在国内大部分医院的开展条件还不够完善。手术操作以及病理相关的假阴性率,也是我国SLNB临床实践中需要面临的挑战。与此同时,针对SLNB的适应证,如何筛选适合行SLNB的患者从而使其免于ALND获得更好的术后生活质量;甚至如何筛选可以免于SLNB的患者都是目前学术领域大胆的尝试。乳腺癌患者腋窝淋巴结的外科处理正围绕着SLNB进行着降阶梯的探索。
本年度前哨淋巴结活检术的研究主旋律集中在以下几个问题:寻求豁免前哨的可行性、新辅助治疗后的SLNB问题、示踪剂选择的新进展。
由ALND到SLNB的降阶梯一直是腋窝淋巴结处理领域的研究热点,然而今年,研究者们又迈出了大胆的一步,将探索的领域拓展到由SLNB到豁免腋窝处理。在这一过程中,我们对低危患者从不同的维度进行着切实准确的筛选。
PS1-07研究:老年低危患者行前哨淋巴结活检术的获益情况
2020年SABCS会议上报道了PS1-07研究结果,197例接受手术治疗但未接受腋窝手术的患者中,有13例(6.8%)发生局部复发,而428例腋窝前哨淋巴结活检的患者中只有7例(1.6%)出现局部复发。这种差异是具有显著性(adj. HR=4.68;95% CI:1.53~14.37)。
当我们结合既往的研究,针对年龄≥70岁,T1-2N0的患者腋窝淋巴结处理选择的两项研究,来自土耳其的Bahadir教授指出在他们自己研究中实施腋窝淋巴结清扫的局部复发率为零,而不实施的为6%;IBCSG研究中,不做腋窝淋巴清扫的局部复发只有3%。

那么哪些老年患者不需要做SLNB呢?一项回顾性研究发现N0,年龄≥70岁,T<2cm,G1-2,LuminalA的患者可以不行SLNB。因此决定老年乳腺癌局部治疗要考虑以下三个方面因素:危险因素,肿瘤的生物学特性,对生存的预期。
ER+T1-2患者是否能根据基因检测结果豁免SLNB
一项单中?回顾性分析研究,入组了2011年11月~2015年12月的绝经后且ER+,HER2-,pT1-2的患者。在纳入的217例患者中,淋巴结状态如下:N0,n=184(85%);Nmi-N1,n=29 (13%);N2-3,n=4(2%)。

结论:SLNB的结果仅改变了4.7%的患者是否接受化疗的决策。更多的时候,SLNB影响化疗方案的选择或局部治疗推荐。基因组图谱在治疗方案制定中的地位越来越重要,SLNB结果在其中的作用正在减弱。如果ER阳性、T1-2 BC和腋窝US阴性的绝经后患者在手术前进行了基因检测,其结果可能会改变手术治疗。对于RS>25的女性,无论SLN状态如何,都建议化疗,但SLN阳性会影响方案推荐。SLNB的结果在RS 18~25岁患者中影响最大。是否在术前使用基因组分析来调整SLNB应该通过前瞻性实验来验证。
这项研究,为免于前哨淋巴结的患者筛选提供了非常好的思路,但是结论中更多地论证了SLNB的结果能否改变RS值的推荐,对于反过来RS值能否左右SLNB的决策谈得并不多。期待其在未来从这一角度展开前瞻性的临床实验。
SOAPET研究:LymphPET检测可豁免前哨淋巴结活检的人群
复旦大学附属肿瘤医院邵志敏教授牵头的前瞻性Ⅱ期研究SOAPET,发现专用腋窝PET(LymphPET)对腋窝淋巴结可以有较好的检测效能。在该研究的第一阶段,临床体检阴性的早期乳腺癌患者,进行LymphPET检测以及常规的腋窝评估(超声、CT等),随后进行规范的腋窝前哨淋巴结活检,验证了LymphPET的检测效能。邵志敏教授团队在2020年SABCS会议上报道了第一阶段的研究结果。
该研究筛选了224例患者,最终成功入组的189例浸润性乳腺癌中,前哨宏转移为40例。临床体检的阴性预测值为78%,超声的阴性预测值为86.3%,而LymphPET(SUV 0.27作为界值)的阴性预测值为87.5。特别值得关注的是,如果将LymphET结合当前常规的临床腋窝评估方式(体检+超声),增加LymphPET可以进一步筛选出80%患者,其腋窝阴性预测值可以高达91%。
我们能够看到,越来越多的来自中国的原研结果在国际会议上大放异彩,该研究在第二阶段将根据LymphPET结果筛选出临床评估腋窝淋巴结阴性的患者,不进行前哨评估,予以随访确认豁免腋窝前哨活检的安全性。期待该研究第二阶段的结果为临床筛选豁免前哨淋巴结活检的患者提供更加精准的评估方式选择。
初始cN0患者中,已有多项研究探索了新辅助后前哨淋巴结活检的可行性和准确性[3],从而避免不必要的ALND,其中最著名的是NSABP B-27[4]和GANEA-2试验[5]。
针对初始cN1患者,曾经无论新辅助治疗的反应如何均推荐采用ALND作为这类患者的标准治疗。然而一部分患者新辅助治疗后的腋窝淋巴结完全缓解,使得这个问题重新引起了大家的重视。其中三阴性肿瘤腋窝淋巴结pCR率达到60%,HER2阳性肿瘤腋窝淋巴结pCR率达到70%,而曲妥珠单抗联合化疗,使得这一比例达到了97%[6][7]。
针对这一问题率先展开研究的是ACOSOGZ1071[8]、SENTINA[9]和SN-FNAC[10]试验。那么在2020年,又有哪些新的研究结果为这一问题提供了新的证据呢?
2020年SABCS会议报道了荷兰的前瞻性、多中心、大样本的RISAS试验结果。RISAS研究在初始腋窝阳性患者新辅助化疗前放置I125粒子,新辅助化疗后采用靶向腋淋巴结切检(TAD)技术进行腋窝评估并进行腋窝清扫术,以验证其准确性。
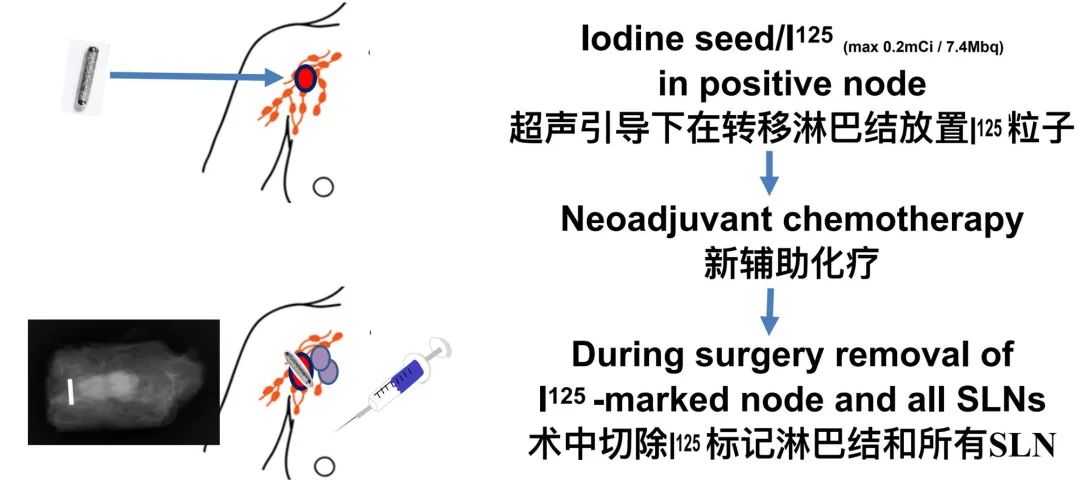
共有252例经病理证实的cN+患者纳入治疗,其中227例接受了RISAS手术/靶向腋淋巴结活检(SLNB联合标记阳性淋巴结切除)。RISAS方法的成功率为98%(223/227)。初步分析显示假阴性率约为5%,阴性预测值约为91%。此外,将SLNB与标记淋巴结切除相结合与单纯SLNB或单独切除标记淋巴结相比,成功率和准确性都得到了提高。
这项前瞻性多中心验证试验表明,在cN+患者NAC术后腋窝分期中,RISAS程序/靶向腋淋巴结切检在成功率和准确性方面更具优势。
一直以来,针对初始cN1患者新辅助治疗后SLNB使用双示踪技术、检出≥2枚阴性SLN时才可以免于ALND [11][12]。由于中国多数医疗机构尚不能选择异硫蓝联合核素双示踪技术进行SLNB,因此,我国临床医生应持谨慎的态度。本研究中,RISAS方法的有效性得到的进一步证实是否能在未来改善我国双标法使用的局限性值得我们期待。
PEONY trial 二次分析探讨双靶治疗后的前哨活检
对于HER2阳性乳腺癌,新辅助治疗前临床腋窝淋巴结阴性患者前哨淋巴结活检的最佳时机尚不明确。此外,对于新辅助治疗后腋窝淋巴结转为阴性患者,前哨淋巴结活检取代腋窝淋巴结清扫的可行性仍存争议。《乳腺癌研究与治疗》(Breast Cancer Res Treat)在线发表我国学者领导的国际多中心PEONY研究的二次分析中探讨了该问题。
此次分析中,临床腋窝淋巴结阴性患者有80例,新辅助治疗后经病理检查淋巴结阴性率为83.8%。新辅助治疗后,对71例患者进行了双示踪剂定位的前哨淋巴结活检,检出率为100%,假阴性率为17.2%。对于新辅助治疗前腋窝淋巴结阳性的患者,曲帕双靶与对照组相比,腋窝pCR率显著提高(P=0.002)。当检出1、2、>2个前哨淋巴结时,假阴性率分别为33.3%、14.3%、0。当检出≥2个前哨淋巴结且金属夹标记淋巴结被切除时,假阴性率为0。
新辅助前腋结阴性、HER2阳性患者新辅助治疗后假阴性率较高,建议进行前哨活检。腋阳性转阴者也存在一定的假阴性。对于双示踪剂定位检出检出≥2个前哨淋巴结且金属夹标记淋巴结被切除的患者,假阴性率极低。
这一研究提醒我们在面对HER2阳性这一特殊患者群体时,在新辅助化疗联合靶向治疗的超高pCR率的鼓舞下,我们应该提高对于前哨淋巴结假阴性的警惕性。同时这组数据也告诉了我们,只要严格执行双标法并且进行足够数目的前哨淋巴结活检,这一部分假阴性能够被我们规避。
目前国内大部分医院开展双示踪法SLNB的条件还不够完善,术者必须具有放射性核素使用资质的要求也让双标法的推广面对着挑战。同时专利蓝、异硫蓝尚未在我国获得临床批准,且核素的临床应用受到严格的管理,在国内尚无法广泛开展,因此中国多选择亚甲蓝、纳米炭、吲哚菁绿作为SLNB示踪剂。
乳腺癌前哨淋巴结示踪剂是定位前哨淋巴结的关键,也是前哨淋巴结活检成功的关键因素之一。在本年度一篇发表在《The American Journal of Surgery》上的一篇来自澳大利亚的meta分析表明,在放射性同位素标记前哨淋巴结显像尚不完善的中心,吲哚菁绿荧光可以作为放射性同位素标记方法的补充或替代。
该研究纳入来自19个研究的2301例患者。吲哚菁绿和放射性同位素在SLN检测(OR=0.90,95%CI:0.66~1.24)或敏感性(OR=1.23,95%CI:0.73~2.05)方面无显著差异。与单独检测放射性同位素I(OR=3.69,95%CI:1.79~7.62)或吲哚菁绿(OR=3.32,95%CI:1.52~7.24)相比,双重检测(ICG+RI)的敏感性明显更好,且研究间无异质性(I2=0%,P=0.004)。吲哚菁绿的在前哨淋巴结示踪上临床应用价值得到了进一步的验证。
随着乳腺癌诊疗技术的不断精进,患者的治愈率正稳步提升,乳腺癌患者治疗后的生活质量的也随之显著提高。SLNB作为一个旨在用更小的损伤获得更加安全的疗效的技术,自其应用至今近30年来,不断的提升着自己在腋窝处理方案中的地位。在未来的研究中,我们将不断在技术上精进腋窝淋巴结活检术的准确性,并且为腋窝处理方案选择中的降阶梯寻找更多的循证医学证据。
1、Latosinsky S,Dabbs K,Moffat F,Evidence-Based Reviews in Surgery G. Canadian AssoCIation of General Surgeons and American College of Surgeons Evidence-Based Reviews in Surgery. 27. Quality-of-life outcomes with sentinel node biopsy versus standard axillary treatment in patients with operable breast cancer. Randomized multicenter trial of sentinel node biopsy versus standard axillary treatment in operable breast cancer: the ALMANAC Trial. Can J Surg 2008;51 (6): 483-485.2、LucCI A,Jr.,Kelemen PR,Miller C,3rd,Chardkoff L,Wilson L. National practice patterns of sentinel lymph node dissection for breast carCInoma. Journal of the American College of Surgeons 2001;192 (4): 453-458. doi: 10.1016/s1072-7515(01)00798-0.3、Shirzadi A,Mahmoodzadeh H,Qorbani M. Assessment of sentinel lymph node biopsy after neoadjuvant chemotherapy for breast cancer in two subgroups: Initially node negative and node positive converted to node negative - A systemic review and meta-analysis. Journal of research in medical sCIences : the offiCIal journal of Isfahan University of Medical SCIences 2019;24 18. doi: 10.4103/jrms.JRMS_127_184、Mamounas EP,Brown A,Anderson S,Smith R,Julian T,Miller B,et al. Sentinel node biopsy after neoadjuvant chemotherapy in breast cancer: results from national surgical adjuvant breast and bowel project protocol B-27. J Clin Oncol. 2005;23:2694–702.5、Classe J-M,Loaec C,Gimbergues P,Alran S,de Lara CT,Dupre PF,et al. Sentinel lymph node biopsy without axillarylymphadenectomy after neoadjuvantchemotherapyis accurate and safe for selected patients: the GANEA 2 study. BreastCancer Res Treat. 2019;173:343–52.6、Hamdy O. Neoadjuvant therapy should be the standard of care for every node positive breast cancer patient. J Breast Cancer. 2019;22:149–52.7、Lyman GH,Temin S,Edge SB,Newman LA,Turner RR,Weaver DL,et al. Sentinel lymph node biopsy for patients with early-stage breastcancer: American SoCIety ofClinical Oncology clinical practice guideline update. J Clin Oncol. 2014;32:1365–83.8、Boughey JC,Suman VJ,Mittendorf EA,Ahrendt GM,Wilke LG,Taback B,et al. Sentinel lymph node surgery after neoadjuvant chemotherapy in patients with nodepositive breast cancer: the ACOSOG Z1071 (Alliance) clinical trial. JAMA. 2013;310:1455–61.9、Kuehn T,Bauerfeind I,Fehm T,Fleige B,Hausschild M,HelmsG,etal. Sentinel-lymph-nodebiopsyinpatientswith breast cancer before and after neoadjuvant chemotherapy (SENTINA):aprospective,multicentrecohortstudy. Lancet Oncol. 2013;14:609–18.10、Boileau J-F,Poirier B,Basik M,Holloway CMB,Gaboury L,Sideris L,et al. Sentinel node biopsy after neoadjuvant chemotherapy in biopsy-proven node-positive breast cancer: theSNFNACstudy. JClinOncol. 2015;33:258–64.11、Zetterlund LH,Frisell J,Zouzos A,Axelsson R,Hatschek T,de Boniface J,et al. Swedish prospective multicenter trial evaluating sentinel lymph node biopsy after neoadjuvant systemic therapy in clinically node-positive breast cancer. Breast cancer research and treatment 2017;163 (1): 103-110. doi: 10.1007/s10549-017-4164-1.12、Zetterlund LH,Frisell J,Zouzos A,Axelsson R,Hatschek T,de Boniface J,et al. Swedish prospective multicenter trial evaluating sentinel lymph node biopsy after neoadjuvant systemic therapy in clinically node-positive breast cancer. Breast cancer research and treatment 2017;163 (1): 103-110. doi: 10.1007/s10549-017-4164-1.
主任医师,教授,博士生导师
中国医科大学附属第一医院乳腺外科主任
辽宁省抗癌协会乳腺癌专业委员会主任委员
中国临床肿瘤学会(CSCO)理事会理事
中华医学会肿瘤分会乳腺肿瘤学组副组长
中国老年学学会乳腺癌分委会副主任委员
北京乳腺病防治学会外科专委会副主任委员
中国抗癌协会乳腺专业委员会常务委员
中华医学会外科分会乳腺癌学组委员
中国医科大学附属第一医院乳腺外科医师,讲师
2008-2017年中国医科大学附属第一医院乳腺外科本硕博连读
2017年至今 中国医科大学附属第一医院乳腺外科
2018年至今中国医科大学医学信息学院博士后在站研究人员





 京公网安备 11010502033352号
京公网安备 11010502033352号