编者按:在2020年12月5-8日,第62届美国血液学会(ASH)年会首次以线上虚拟会议的形式举行。在这项血液学“盛宴”汇聚了全球各地的血液肿瘤专家和学者,多项重磅级的研究公布了临床数据。本次会议上来自华中科技大学同济医学院附属同济医院周剑峰教授所在团队开创的利用双靶点CAR-T技术鸡尾酒疗法治疗复发、难治性B细胞淋巴瘤患者入围本次会议口头报告。《肿瘤瞭望》特邀周剑峰教授解答本研究中热点问题。
大剂量化疗后自体干细胞移植(HDT-ASCT)是复发性或难治性(R/R)B细胞淋巴瘤的标准治疗。HDT-ASCT的合格性是基于存在对挽救治疗化疗敏感的疾病。ASCT前PET扫描阳性的患者的生存率显著较低。此外,挽救治疗后疾病进展的患者的结局极为不佳。我们假设,HSCT后,清髓性预处理将减少免疫抑制微环境,并且在造血重建期间给予CAR-T细胞治疗可以根除移植后残留疾病,从而降低HSCT后的复发率。基于我们以前的工作,即靶向CD19和CD22的序贯细胞输注的双靶向CAR T细胞鸡尾酒疗法可能有助于克服B细胞恶性肿瘤的抗原逃逸复发,
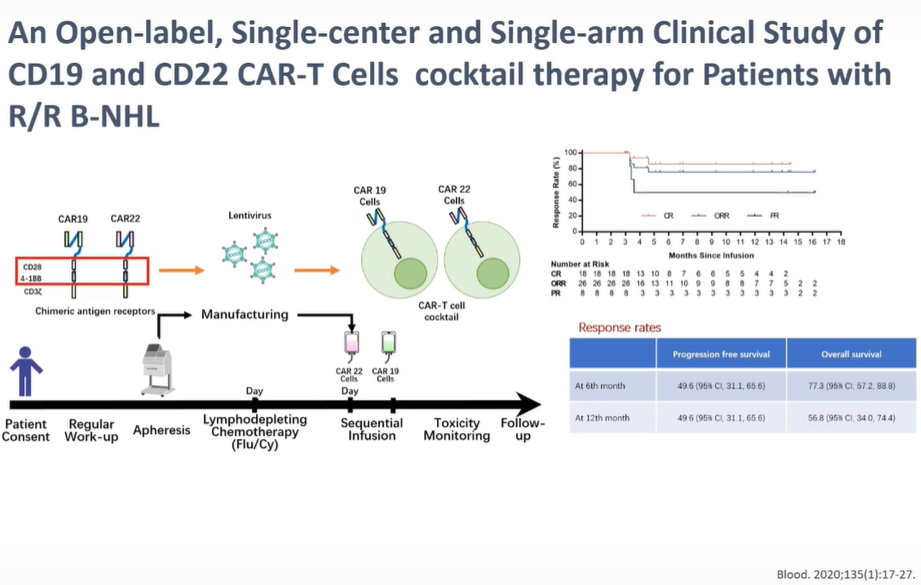
#618.CD19/CD22 CAR-T Cell Cocktail Therapy Following Autologous Transplantation in Patients with Relapsed/Refractory B-Cell Lymphomas
复发性/难治性B细胞淋巴瘤患者自体移植后接受CD19/CD22 CAR-T细胞鸡尾酒疗法的疗效评估
我们进行了一项开放标签、单中心、以及在自体造血干细胞移植(HSCT)后序贯输注CD22和CD19 CAR-T细胞的治疗的单组初探性研究。旨在评价挽救治疗后疾病残留或进展的R/R B细胞淋巴瘤患者治疗的安全性和疗效。
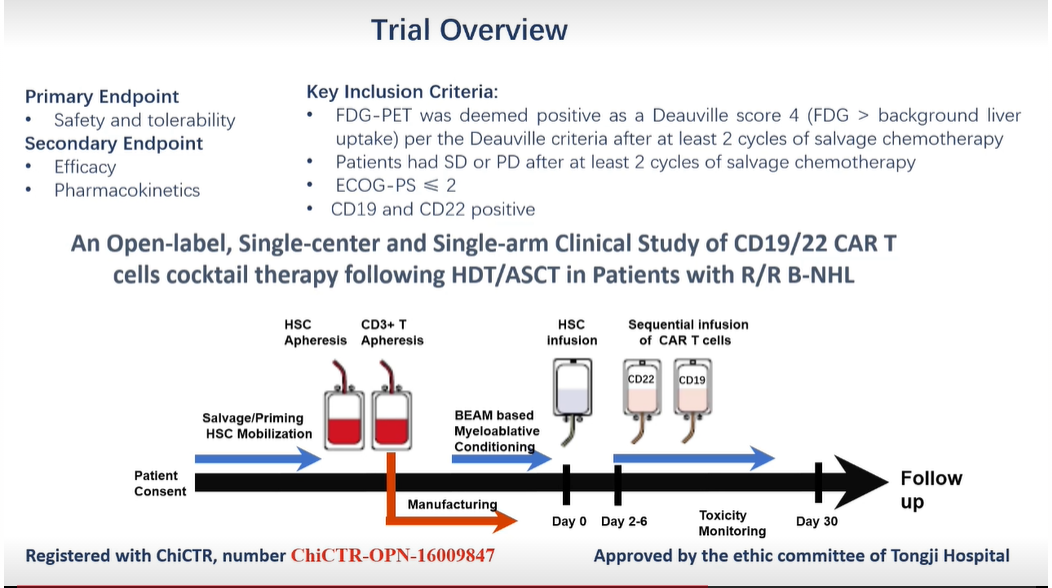
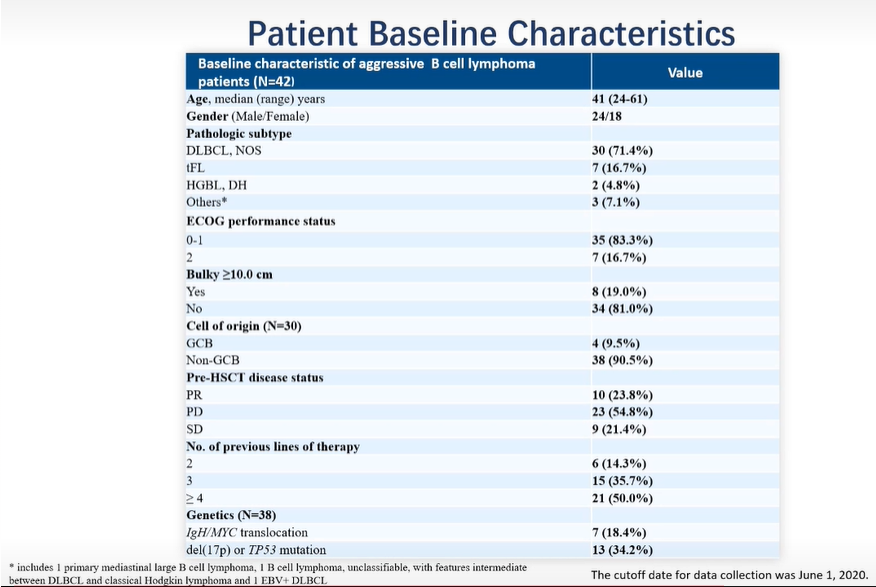
2016年11月14日至2019年8月15日期间,共纳入42例患者接受了BEAM方案预处理后的自体造血干细胞移植(HSCT),随后接受了CAR 19/22 T细胞输注。
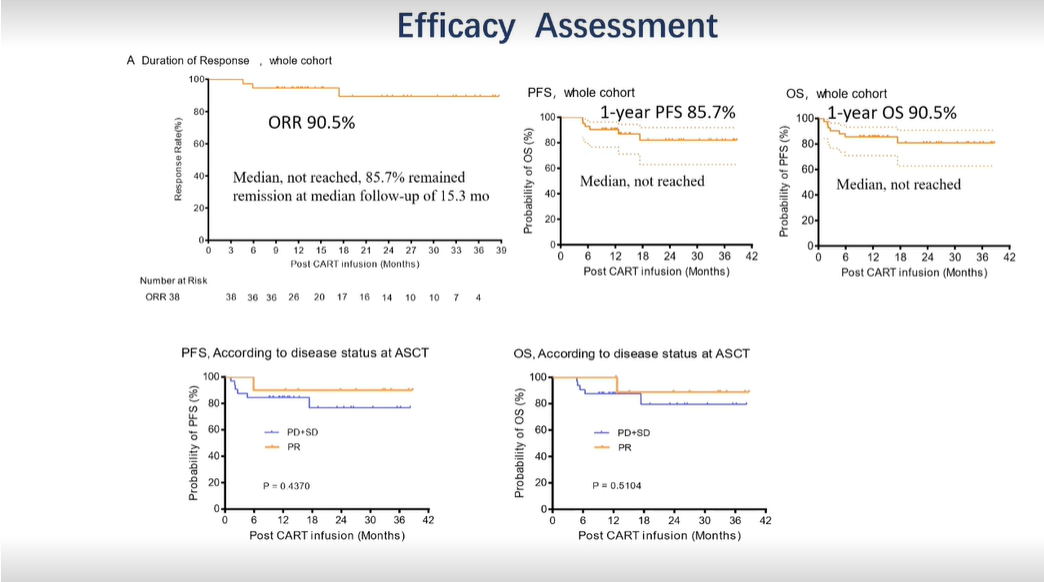
有效性方面:总有效率为90.5%(95%CI,77.4-97.3)。中位随访13.8个月,未达到中位无进展生存期(PFS)和总生存期(OS)。12个月PFS率为85.7%(95%CI,70.9-93.3)。
安全性方面:仅2例(5%)患者发生3级细胞因子释放综合征(CRS)。21%的患者发生任何级别的神经毒性,5%为重度3级。所有CRS和神经毒性均可逆。
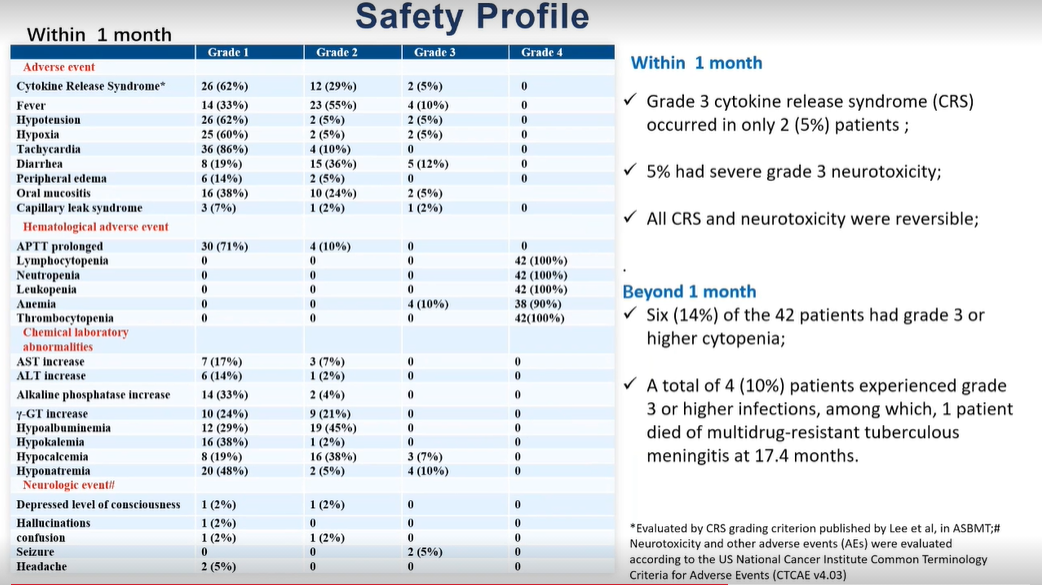
除了极高的完全缓解率,本研究中研究的自体HSCT加CD19/CD22 CAR-T细胞鸡尾酒疗法的缓解持久性和低毒性强调了这种清髓性预处理和R/R B细胞淋巴瘤的双靶向方法的强大潜力。
《肿瘤瞭望》:今年 ASH 大会上,CD19/CD22 CAR-T 鸡尾酒疗法作为口头报告登场,且我们注意到 3 级细胞因子释放综合征(CRS) 仅 2(5%)例发生,总有效率为 90.5%(95% CI, 77.4-97.3),显示低毒副作用以及长时间缓解的疗效,可否请您为我们介绍下本实验的亮点 (给药方案)和意义?
周剑峰教授:的确,这一研究设计之初,作为研究人员的我们也顾虑重重。首先实验设计的方案较为复杂,首先进行患者的化疗诱导后进行的自体移植接着再给予两种不同靶点的CAR-T细胞,开始我们也会担心这一方案是否会有较大的副作用,但实际结果来看包括CRS以及神经相关毒性都比较轻微。究其原因,其实CRS主要是因为体内形成记忆的巨噬细胞和T细胞导致的,而患者通过了自体移植前的化疗已经清除原有的免疫微环境,因此患者的重度的免疫风暴和不良反应显著降低。目前这一治疗模式在我们中心已经比较普遍且广泛应用。
《肿瘤瞭望》:我们注意到患者都接受 BCMA 方案后进行HDT-ASCT,能否请您谈一谈入组患者的标准,包括不同年龄、性别、接受既往治疗情况不同的患者是否有相同获益?是否存在 biomarker 来衡量患者的疗效情况呢?
周剑峰教授:这一问题具有现实意义,实际上在研究过程中我们发现即使经过一定的治疗,患者仍存在“天花板”效应,约有10%的患者未能通过这一方案获益,我认为主要存在以下三点原因:1.患者的靶点,如CD19缺失或突变,CD22呈弱表达。2.患者先天T细胞情况较差,输注入体内的T细胞扩增情况不好,T细胞存活状态不理想。这是自身T细胞的因素决定的,在T细胞杀伤肿瘤细胞的能力上存在限制3.特殊的淋巴瘤比如伯基特淋巴瘤以及肿瘤位置较差,如处于中枢神经等部位。相较于普通的R/R B细胞淋巴瘤患者来说更困难。
对于这些患者的biomarker也是基于以上三点:1.在治疗前清楚患者靶点表达状况2.评估T细胞功能(目前这一技术还尚需完善)3.肿瘤部位或病理类型是否特殊。这些问题对整体治疗和预后至关重要。
《肿瘤瞭望》:虽然截止目前本研究PFS、OS 还未达到,但这一疗法潜力巨大,在未来CD19/CD22 的CAR-T 双抗疗法还会开展哪些临床研究,本试验后续是否会开展扩展队列研究呢?
周剑峰教授:从这一研究现阶段结果来看,治疗前景十分广阔,因此后续一定会开展相关研究,但美中不足的是研究设计之初还是存在一些问题。第一此次研采用的是序贯治疗模式,但这在未来标准化产品中不容易达到,因此后续研究可能会改为双靶点(同时靶向CD19/22)同时进行。第二由于刚刚提到的患者存在“天花板”效应,因此未来还需要找寻更加有效的技术方案使得更多患者能够获益。第三研究还处于单中心,未来在其他中心是否能重复,这一方案是否能够推广也是目前面临的问题之一。
二级教授,主任医师,博士生导师
华中科技大学同济医学院附属同济医院血液科主任
教育部重点实验室同济医院肿瘤生物医学中心副主任
国家杰出青年基金获得者
现任中华医学会血液分会常务委员,实验诊断学组副组长,中国抗癌协会血液肿瘤专业委员会副主任委员,青年委员会主任委员,中国基因治疗协会委员,中国实验血液学会委员。任中华血液学杂志,中国实验血液学杂志,临床血液学杂志,白血病·淋巴瘤,国际输血及血液学杂志等学术杂志编委,国家自然科学基金终审评委。
主要专业方向:白血病,淋巴瘤的分子诊断和个体化治疗。在国际期刊如Blood,Nature Genetics, J Exp Med,JNCI 等共发表专业论文70余篇,影响因子> 200分,近5年论文的SCI 总引用一千余次。
?





 京公网安备 11010502033352号
京公网安备 11010502033352号