编者按:转移性尿路上皮癌(mUC)是目前免疫治疗的热点领域。一线铂类化疗是mUC的标准治疗,但由于肿瘤进展较快,患者化疗有效的维持时间较短,因此需要探索一线化疗后维持期治疗策略,以进一步改善患者的肿瘤控制。今年ASCO大会上公布的Jevelin Bladder 100研究,针对mUC一线铂类化疗有效的患者,在化疗结束后维持期使用PD-L1抗体Avelumab,使患者PFS和OS显著获益,该结果引起了轰动,并发表在NEJM上。在2020年ESMO大会上,本研究带来了进一步的亚组分析(摘要号704MO)和生物标记物(摘要号699O)研究的结果,为进一步探讨优势人群提供了线索。北京大学第一医院虞巍教授与我们分享如下。

中国医疗保健国际交流促进会肾脏移植分会青年委员会委员
Jevelin Bladder 100研究是国际多心Ⅲ期临床研究,研究入组的不可切除UC或mUC接受铂类化疗4-6个周期,肿瘤评估有效才进入本研究,随机分为最佳支持治疗+Avelumab和最佳支持治疗+安慰剂组,主要观察终点是OS。本研究共纳入了700例患者。研究结果显示,Avelumab组和安慰剂组的中位OS为21.4个月和14.3个月(HR=0.69,95%CI:0.56~0.86,P<0.001),PFS3.7个月和2.0个月(HR=0.62,95%CI:0.52~0.75),PD-L1+的患者OS分别为NE和17.1个月(HR=0.56,95% CI:0.40~0.79,P<0.001),PFS为5.7个月和2.1个月(HR=0.56,95%CI:0.43~0.73)。正是因为此研究结果的突破性进展,NCCN指南迅速推荐将Avelumab作为一线铂类化疗有效患者维持期治疗。
 ▲Jevelin Bladder 100研究设计
▲Jevelin Bladder 100研究设计
在本次ESMO大会上,该研究更新了随访数据,两组的OS分别达到了25.3个月和16.5个月,PFS为4.6个月和2.0个月。OS的亚组分析,对于年龄65岁以上,ECOG 0,PD-L1+,没有内脏转移,没有肝转移,没有肺转移的患者生存获益更为显著。因此,该研究证实了一般状况良好、没有内脏转移、PD-L1+的患者是免疫治疗的优势人群这一理念;并且在进一步的随访数据显示,PFS超过一年的患者,其肿瘤控制获得长期稳定,显示了免疫治疗的远期疗效较好的特点。
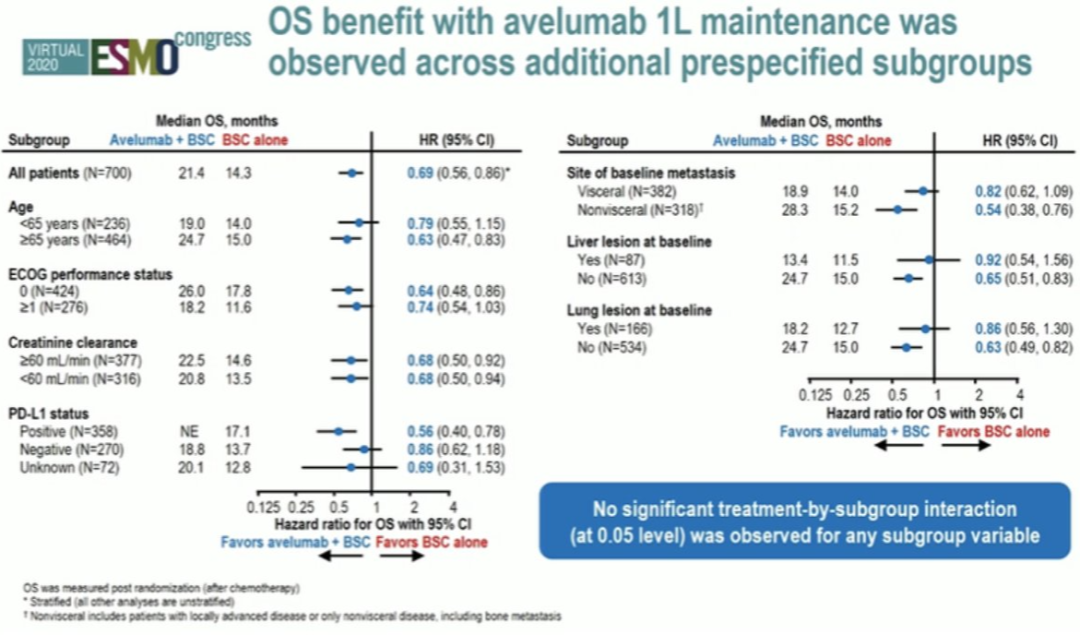 ▲Jevelin Bladder 100研究亚组分析
▲Jevelin Bladder 100研究亚组分析
由于化疗与免疫治疗的机制不同,因此该研究还报告了化疗的疗效对于免疫治疗的影响。在研究入组的患者中,对铂类化疗达到CR的患者,两组的中位OS均未达到,Avelumab组可能具有优势(HR=0.81),PFS分别为7.4个月和3.8个月(HR=0.65)。对于化疗后PR患者,两组OS分别为19.2个月和12.1个月(HR=0.62),PFS分别为3.1个月和1.9个月(HR=0.58),。因此,对于不同化疗反应而言,Avelumab都能进一步改善肿瘤控制,对于PR的患者,其相对获益更为显著,符合研究设计之初二线免疫治疗前移至维持期更能获益的设计思想。
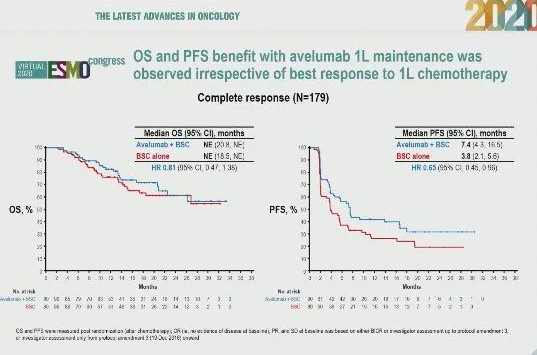 ▲化疗后完全缓解(CR)患者的OS获益
▲化疗后完全缓解(CR)患者的OS获益
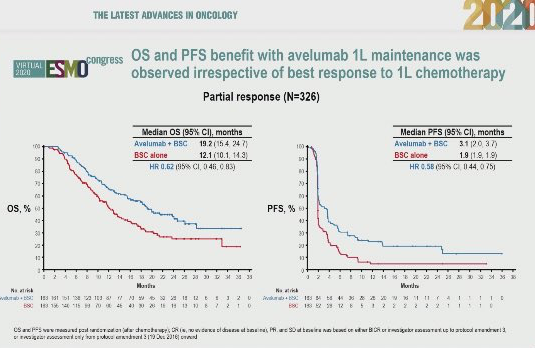 ▲化疗后部分缓解(CR)患者的OS获益
▲化疗后部分缓解(CR)患者的OS获益
目前,4项有关mUC一线免疫治疗的Ⅲ临床研究已经公布结果,包括KEYNOTE 361、IMvigor130、DANUBE、Javelin Bladder 100。在这四项研究结果中,最为成功的是化疗后免疫维持的Javelin Bladder 100,而一线化疗直接联合免疫的KEYNOTE 361和IMvigor130的研究结果显示联合可能有优势,但获益程度较小,结果差强人意。
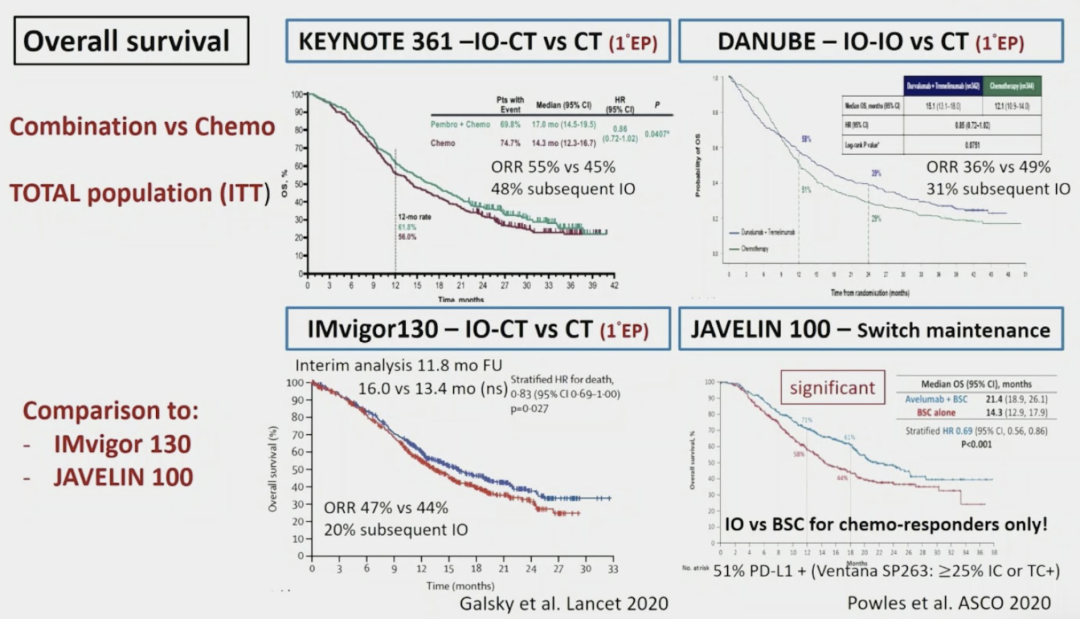 ▲四项一线免疫治疗研究ITT人群OS汇总
▲四项一线免疫治疗研究ITT人群OS汇总
 ▲四项一线免疫治疗研究PD-L+人群OS汇总
▲四项一线免疫治疗研究PD-L+人群OS汇总
出现一线联合研究的数据不如一线维持效果好的原因较为复杂,可能与一线维持Javelin Bladder 100研究的入组患者是铂类化疗有效的患者有关,铂类化疗敏感的患者中有一部分(如存在DNA损伤修复基因缺陷)也是对免疫治疗反应较好的人群,化疗的疗效有助于筛选免疫治疗的优势人群。
反观,KEYNOTE 361和IMvigor130研究的雄心更大,希望做到一线全人群的覆盖,但由于mUC的异质性很强,并且有相当一部分患者的恶性程度较高,对化疗和免疫治疗都耐药,一线纳入这部分人群,会导致整个临床研究的结果在统计上出现理想结果的困难加大。CTLA-4联合PD-L1抗体的的联合免疫研究DANUBE的结果显示联合免疫在治疗早期的生存劣于化疗,但长期随访的生存数据更好,存在生存曲线交叉的现象,联合免疫治疗的ORR也弱于化疗,因此,对于ORR要求较高一线mUC的患者而言,联合免疫的临床运用前景欠佳。考虑免疫治疗的长期生存优势,在顺铂不耐受的患者中是未来的研究方向,尤其是在生物标记物(如TMB、PD-L1)指导下,免疫单药和联合免疫治疗依然可能具有较好的临床运用前景。
在本次大会报告中,Javelin Bladder 100研究也探讨了分子标记物在免疫治疗疗效预测中的作用。由于免疫治疗的疗效与肿瘤的免疫微环境密切相关,因此其疗效与免疫相关信号通路可能具有一定关系。在研究随机入组前,部分患者接受了穿刺活检,检测了PD-L1和CD8+IHC表达情况,进行全外显子、转录组和TCR测序,并结合血液中免疫相关指标,分析了免疫治疗的疗效与这些免疫标记物的相关性。
TMB已经作为泛瘤种多线治疗后的标记物获得了FDA的批准。这项探索性分析显示,在TMB高于中位值的患者中,Avelumab组的HR为0.48,而在低于中位值患者中HR为0.88。联合TMB和PD-L1的状况,高TMB和PD-L1+的患者的获益显著优于低TMB和PD-L1-的患者,HR分别为0.51和1.27。在一线化疗联合免疫的IMvigor130研究的分析中,同样也证实了对于高TMB和PD-L1+的患者,在化疗基础上联合免疫依然是获益更为显著的人群。因此,TMB和PD-L1在mUC患者中预测化疗联合免疫,单药免疫治疗的疗效的作用依然值得进一步探索,有助于选择临床上更能获益的人群,制定针对性的治疗策略。
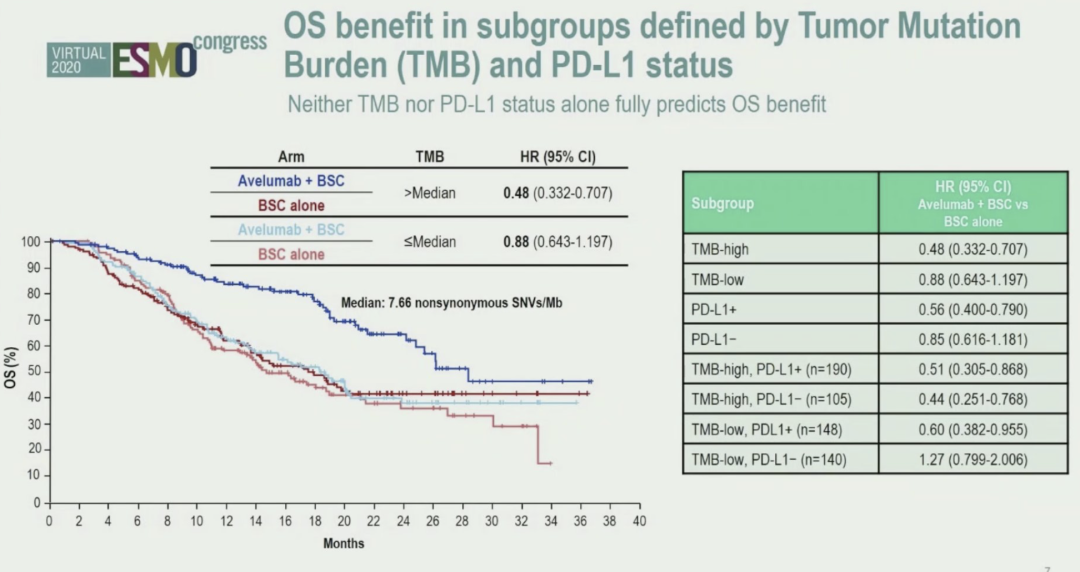 ▲根据TMB和PD-L1状态分层的OS获益
▲根据TMB和PD-L1状态分层的OS获益
在免疫相关信号通路基因异常方面,本研究纳入分析了既往研究比较关注的Notch通路、Hedgehog通路、TGF-beta通路、血管生成通路。疗效分析显示,无论这些通路的表达状况,使用Avelumab作为维持治疗均能使患者生存获益,这些通路表达水平高于中位值的患者,其生存获益是减少的,提示免疫抑制环境的存在可能减弱免疫治疗的疗效。而在各免疫细胞活化相关的基因表达分析中,高表达的患者整体生存获益更为显著,提示,免疫细胞的活化有助于免疫治疗疗效的发挥。
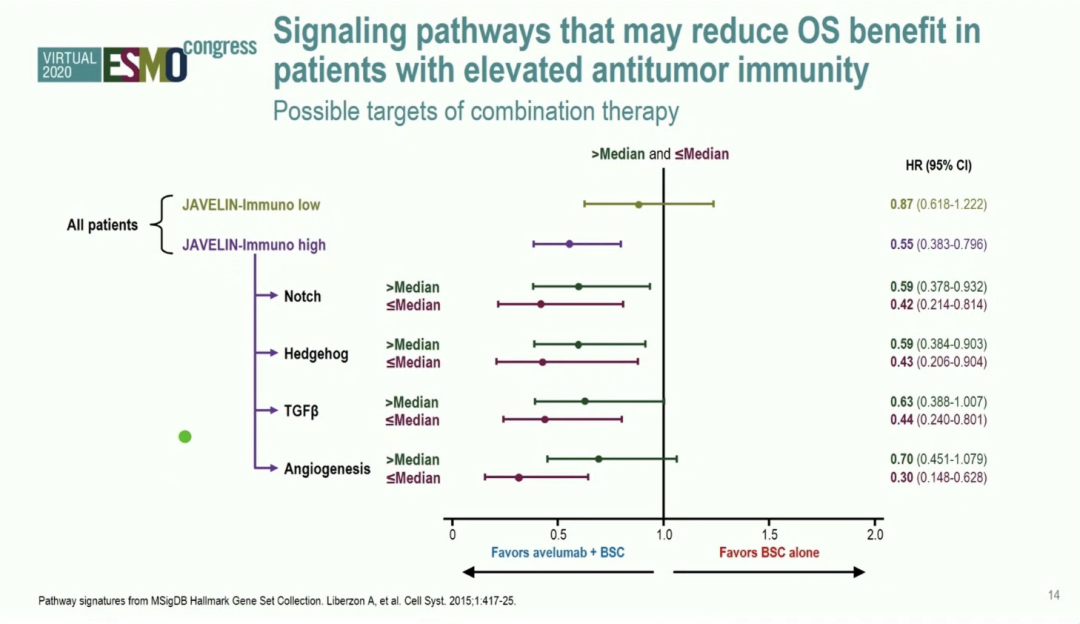 ▲不同通路信号上调可减少OS获益
▲不同通路信号上调可减少OS获益
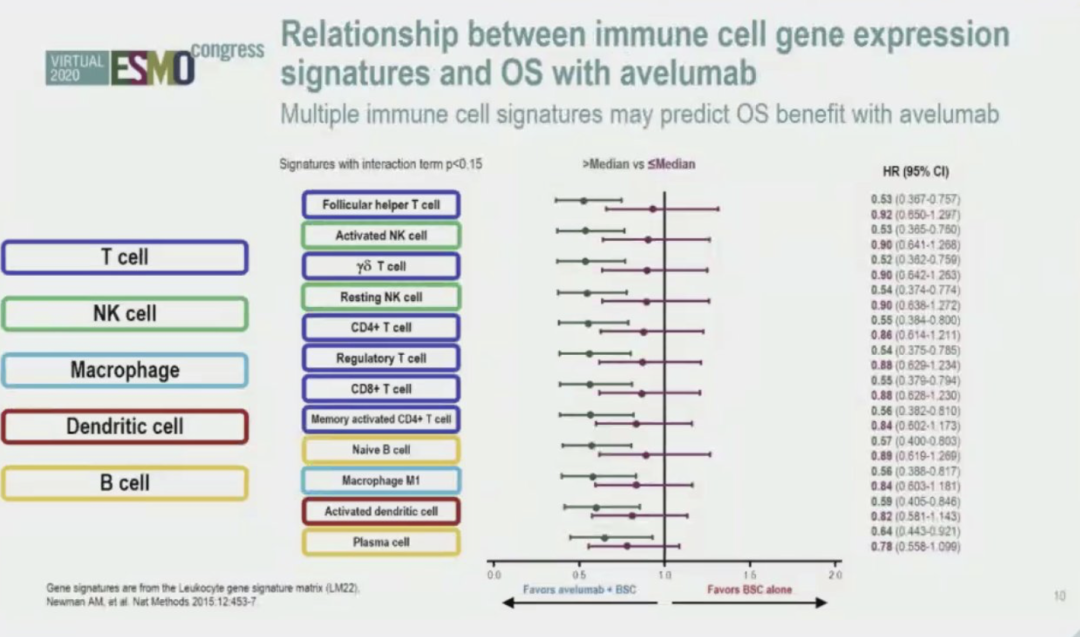 ▲免疫细胞基因表达与阿维鲁单抗OS相关性
▲免疫细胞基因表达与阿维鲁单抗OS相关性
在检测不同突变标记和DNA损伤修复基因突变的分析中依然发现,对于存在更多突变标记和DNA损伤修复基因阳性的患者,免疫治疗的疗效更好,这与TMB作为生物标记物的指导思想是一致的,即突变越多,产生新抗原的可能越大,对免疫治疗的疗效可能更好。
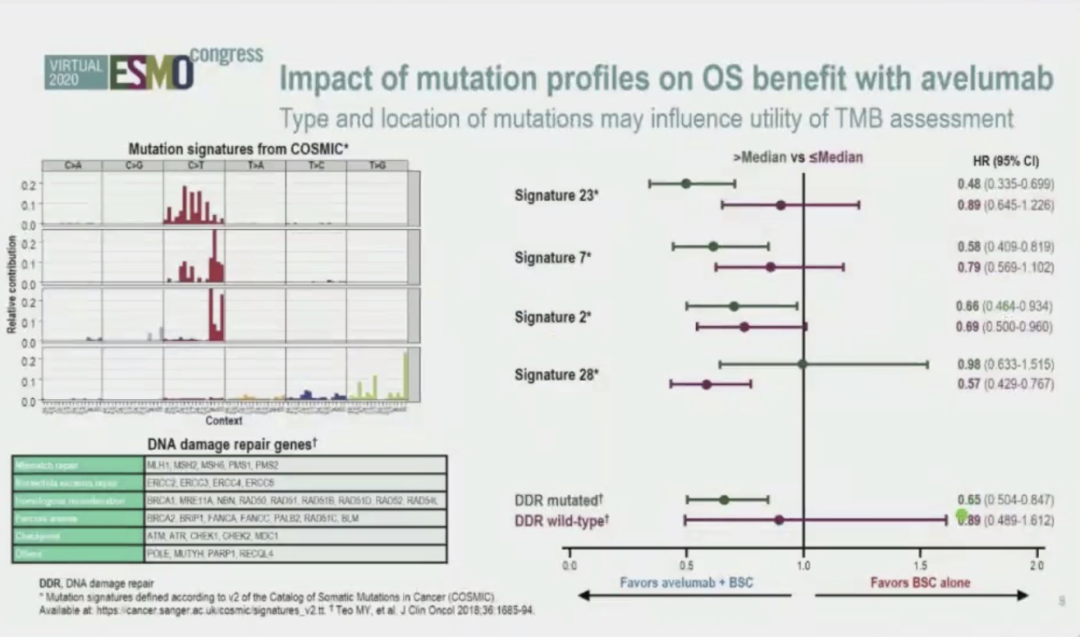 ▲突变谱对阿维鲁单抗OS获益的影响
▲突变谱对阿维鲁单抗OS获益的影响
在ASCO 2020的大会上,报告了IMvigor130研究基于分子标记物的研究结果,其检测的立足点与Javelin Bladeer 100研究是一致的,考虑了PD-L1 表达、TMB水平、突变标记、抑制性免疫炎症环境。该研究也证实在免疫治疗中,免疫活性高,抑制细胞因子活性较少的肿瘤是免疫治疗的优势人群。将来可能在这些分子标记物的指导下,设计新的临床研究,探讨,化疗,免疫在不同患者的中疗效,制定风险获益比,性价比更好的治疗策略。
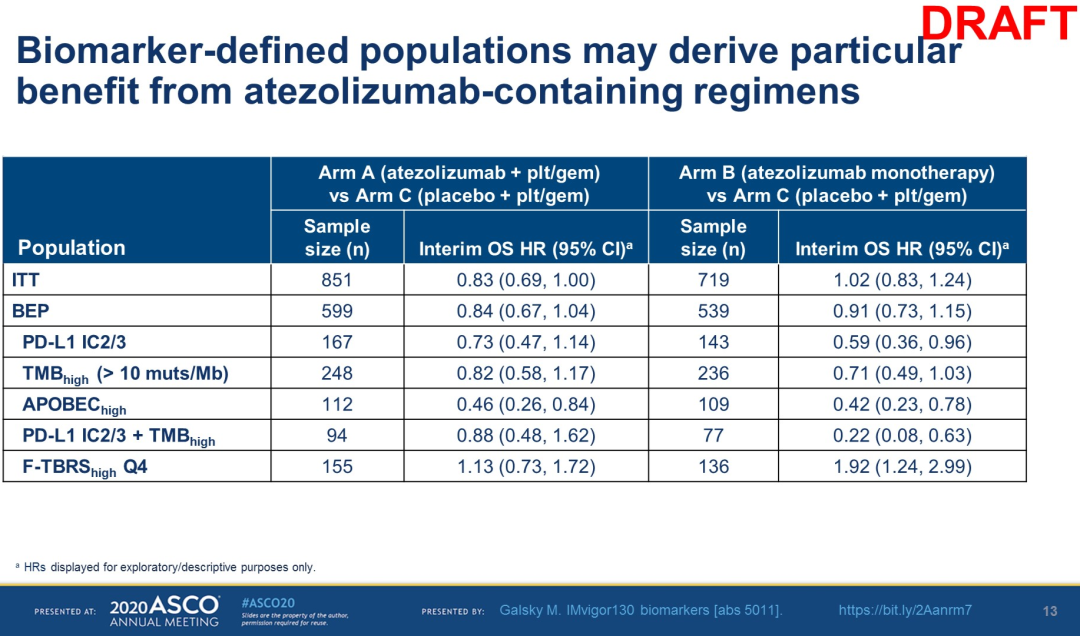 ▲IMvigor130研究中的分子标志物分析
▲IMvigor130研究中的分子标志物分析
综上所述,在mUC患者中,Javelin Bladeer 10研究将免疫治疗从二线治疗向化疗有效一线维持阶段推进,在化疗CR和PR中均能改善肿瘤控制,在PR的患者中获益更为显著。这一结果将会迅速改变目前的临床实践。在分子标记物领域,随着对肿瘤基因层面和免疫微环境的认识提高,对于免疫治疗的优势人群的认识越来越深入,相信这些研究将更好的指导今后临床实践。





 京公网安备 11010502033352号
京公网安备 11010502033352号